Hoy en día, la α-sinucleína ha sido el foco principal para comprender la etiología de una familia de trastornos neurodegenerativos superpuestos denominados α-sinucleinopatías. Estas incluyen la enfermedad de Parkinson (EP), la demencia con cuerpos de Lewy, la enfermedad de Alzheimer, la atrofia multisistémica y la neurodegeneración con acumulación de hierro en el cerebro tipo 1. La α-sinucleína es una proteína de 14 kDa que está altamente expresada en el sistema nervioso y su función está asociada al recambio de vesículas sinápticas y la liberación de neurotransmisores. La característica distintiva de las α-sinucleinopatías es la presencia de inclusiones intracelulares proteicas que contienen agregados mal plegados de α-sinucleína en neuronas y células gliales. Sorprendentemente, las α-sinucleinopatías producen parkinsonismo clínico, pero implican diferentes líneas de tiempo de déficit cognitivo y, en algunos casos, las inclusiones de α-sinucleína se desarrollan en células y áreas cerebrales diferentes de las afectadas por la EP típica. Una plétora de estudios ha demostrado que la sobreexpresión o los tratamientos in vivo/in vitro con α-sinucleína causan una serie de procesos secundarios que resultan en neuroinflamación, transmisión sináptica alterada, deterioro cognitivo y muerte celular.

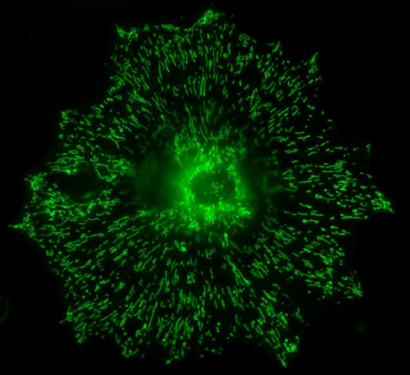
Expresión de panexones en membrana plasmática de astrocito
A pesar de esta evidencia, los mecanismos subyacentes a la acción patológica de α-sinucleína aún no se han aclarado por completo. Hasta ahora, la mayoría de los estudios se han centrado en los efectos de α-sinucleína en las neuronas, mientras que la participación de los astrocitos ha recibido una atención menor. En consecuencia, nuestro Laboratorio se ha enfocado en dilucidar los mecanismos por los cuales los astrocitos podrían contribuir a las acciones patológicas evocadas por α-sinucleína. En particular, tratamos de entender la contribución de dos familias de canales de la membrana plasmática (hemicanales y panexones) en las alteraciones cerebrales inducidas por α-sinucleína en tres aspectos fundamentales: funciones astrocíticas y neuronales, comunicación de astrocitos con las neuronas y sobrevida celular.
Los hemicanales y panexones son canales de la membrana plasmática permeables a iones y pequeñas moléculas que permiten el intercambio difusional entre los compartimentos intra y extracelulares, lo que permite la liberación de sustancias de relevancia biológica (ATP, Ca2+ y glutamato). Sin embargo, se ha demostrado que diferentes agentes patológicos exacerban la apertura normal de los hemicanales y panexones astrogliales. Esto último se ha asociado a alteraciones en la homeostasis del Ca2+ intracelular y la subsecuente liberación de grandes cantidades de gliotransmisores que podrían inducir neurotoxicidad. En este contexto, dado que los hemicanales/panexones son permeables al Ca2+ y su apertura está controlada por el Ca2+ intracelular, especulamos que la α-sinucleína podría incrementar la actividad de hemicanales/panexones astrogliales, deteriorando la homeostasis Ca2+ y la propia función del astrocito con consecuencias significativamente deletéreas para la transmisión sináptica y la sobrevida neuronal.
La α-sinucleína reduce el tamaño de mitocondrias en astrocitos
Lecturas de profundización:
*Díaz EF, Labra VC, Alvear TF, Mellado LA, Inostroza CA, Oyarzún JE, Salgado N, Quintanilla RA, Orellana JA. Connexin 43 hemichannels and pannexin-1 channels contribute to the α-synuclein-induced dysfunction and death of astrocytes. Glia. 2019;67(8):1598-1619. Descargar documento en pdf
*Avudara V, Retamal MA, Del Rio R, Orellana JA. Synaptic functions of hemichannels: A double-edged sword. Frontiers in Molecular Neuroscience. 2018. 11:435. Descargar documento en pdf


No responses yet